“幽门螺杆菌胃炎京都全球共识”解读
上海交通大学医学院附属仁济医院消化内科 刘文忠
2014 年1 月31 日-2 月1 日,由全球40 余位相关领域专家参加的“幽门螺杆菌(Helicobacter pylori, Hp)胃炎全球共识”会议在日本京都召开。经过会前准备后,会议上采用Delphi 法、无记名电子投票系统,对预先准备的4 部分内容[ 与国际疾病分类(International Classification of Diseases,ICD)-11 相关的胃炎分类;Hp 感染相关消化不良;胃炎的诊断;胃炎的处理]的23 个临床问题和相关陈述进行表决,就其中22 个问题和相关陈述达成了共识。为方便解读、避免内容重复、增强可读性和便于理解,本文未根据共识原文中的4 部分内容和临床问题以及相关陈述按序解读。22 个临床问题和相关陈述参见附件。
一、Hp 胃炎是一种感染性疾病
Hp 感染是人类最常见的慢性感染之一,感染后一般难以自发清除而导致终身感染,除非进行根除治疗,或胃黏膜发生严重肠化生时细菌难以定植(Hp 只能定植于胃型上皮),才会自动消失。
1、即使患者没有症状,也不论有无消化性溃疡、胃癌等并发症,Hp 胃炎应被定义为一种感染性疾病【陈述6】
组织学上,慢性胃炎的定义是胃黏膜有淋巴细胞、浆细胞浸润,“ 活动性”则是指胃黏膜有中性粒细胞浸润。目前已清楚,几乎所有Hp 感染者在组织学上均存在慢性活动性胃炎( chronic activegastritis)[1-3]。Hp 感染诱发的慢性活动性胃炎,即Hp 胃炎(Hp gastritis),是Hp 感染的基础病变,在此基础上,部分患者可发生消化性溃疡( 十二指肠溃疡、胃溃疡)、胃癌以及胃黏膜相关淋巴样组织(MALT)淋巴瘤等严重疾病,部分患者可有消化不良症状[4-5]。总体上,约70%的Hp 感染者既无消化不良症状,也无严重病变。但重要的事实是,Hp 胃炎,不论有无症状或有无并发症,几乎均存在活动性胃炎,即存在胃黏膜病理变化。因此,将Hp 胃炎定义为感染性疾病(Hp 感染后至少诱发慢性活动性胃炎),即使患者没有症状,也不论有无消化性溃疡、胃癌等并发症,是客观、合理的。
2、将Hp 胃炎定义为一种感染性疾病是迟到的共识
Hp 研究诺贝尔医学奖得主之一病理科医师Warren 在1979 年就注意到胃黏膜中细菌的存在与慢性胃炎活动性相关。随后有不少观察研究证实,几乎所有Hp 感染者均在组织学上存在慢性活动性胃炎。但Hp 感染与慢性活动性胃炎之间存在正相关,并不能说明两者之间存在因果关系。要证明是Hp 感染引起慢性活动性胃炎,必需符合柯赫法则(Koch’s postulates),即符合确定病原体为疾病病因的4 项条件:①该病原体存在于所有该病患者中;②该病原体分布与体内病变分布一致;③清除病原体后疾病可好转;④在动物模型中,该病原体可诱发与人类相似的疾病。大量研究表明:①80% ~95%的慢性活动性胃炎患者胃黏膜中有Hp 感染, 5% ~20%的阴性率反映了慢性胃炎病因的多样性;②Hp 分布以胃窦为主,与胃内炎症分布一致;③根除Hp 可使胃黏膜炎症消退;④已在志愿者和动物模型中证实Hp 感染可引起胃炎。上述4 项条件在1985 年Hp 研究诺贝尔医学奖得主之一Marshall 医师本人作为志愿者吞服培养的Hp,证实可以诱发胃炎后就已得到满足[6]。Harrison 内科学早就在其感染性疾病栏目中加入了Hp 感染。
3. Hp 胃炎实际上是一种传染病
Hp 可以在人-人之间传播[7]。感染者和可能包括被污染水源是最主要的传染源。口-口和粪-口是其主要传播途径,以口-口传播为主。前者主要通过唾液在母亲至儿童和夫妻之间传播,后者主要通过感染者粪便污染水源传播。儿童和成人均为易感人群。感染性疾病分为传染性和非传染性,因此Hp胃炎定义为传染病更为确切( infectious disease 既可译为“感染性疾病”,也可译为“传染病”)。
4. 世界卫生组织( WHO)ICD 中的胃炎分类应调整【陈述1】【陈述2】
Hp 感染是慢性胃炎最主要的病因。WHO 的ICD-10 版(1989 年制订)胃炎和十二指肠炎(K29)分类中未提及Hp,这一版本显然已经过时。ICD-11 版目前仍处于草拟阶段。Hp 胃炎京都全球共识(简称“京都全球共识”)提议,根据病因进行胃炎分类,将Hp 诱发的胃炎(Hp-induced gastritis)置于感染性胃炎头条。毫无疑问,这样的分类更为客观、合理。
二、Hp 感染与消化不良
消化不良( dyspepsia)主要指上腹部疼痛或不适,后者包括餐后饱胀、早饱、上腹烧灼感、上腹胀气、嗳气、恶心和呕吐,是一组临床上很常见的症候群,人群中约10% ~ 20% 的个体存在消化不良[8],我国因消化不良就诊的患者占普通内科门诊就诊者的10%,占消化科门诊就诊者的50%。为此,消化不良的处理耗费了大量医疗资源,合理的处理对于节约医疗资源具有重要作用。消化不良经相关检查后,可分为器质性和功能性两类,后一类消化不良占大多数。传统的消化不良原因归类中,一般不将慢性胃炎(包括Hp 相关慢性活动性胃炎)作为器质性消化不良的原因[9],因为多数慢性胃炎患者无症状,有症状者其症状与慢性胃炎严重程度的相关度亦较低。
1. Hp 胃炎是部分消化不良患者症状的原因【陈述7】
Hp 胃炎可以在部分患者中产生消化不良症状,这一结论的证据来自三方面:①志愿者研究:曾有3名志愿者吞服Hp,证实可以诱发胃炎和消化不良症状[6,10]。②根除治疗对消化不良症状的影响:不少安慰剂对照研究发现,根除Hp 对Hp 胃炎患者消化不良症状的疗效较安慰剂高约10%[11],部分患者症状可获得长期缓解。需要指出的是,在消化不良处理的各种策略中,目前有安慰剂对照大样本研究证实疗效的仅仅是根除Hp 和质子泵抑制剂( PPI)治疗。③相关机制研究:Hp 胃炎患者存在胃肠激素(胃泌素、ghrelin)水平改变,影响胃酸分泌;炎症可导致胃十二指肠高敏感和运动功能改变。这些改变可以解释消化不良症状的产生[11]。可以类比的是,感染可诱发肠易激综合征,即感染后肠易激综合征( post-infectious irritable bowelsyndrome)和感染可诱发消化不良,即感染后消化不良( post-infectious dyspepsia),两者均已成为共识, Hp 胃炎可导致消化不良也应该成为共识。为什么不是所有Hp 胃炎患者均产生消化不良症状呢?这一情况类似于Hp 感染诱发的消化性溃疡,感染者中也仅有15% ~ 20% 的个体发生溃疡。这是由于Hp 胃炎患者产生消化不良症状或消化性溃疡,除Hp 感染外,尚需其他因素(遗传因素、环境因素、精神/ 心理因素等)参与。
2. Hp 相关消化不良是一种独特实体( distinctentity)【陈述8A】【陈述8B】
Hp 胃炎伴消化不良症状患者根除Hp 后基于症状变化情况可分为3 类:①消化不良症状得到长期缓解;②症状无改善;③症状短时间改善后又复发。目前认为第一类患者属于Hp 相关消化不良(Hp-associated dyspepsia),这部分患者的Hp 胃炎可以解释其消化不良症状,因此不应再属于罗马Ⅲ标准定义(无可以解释症状的器质性、系统性和代谢性疾病)的功能性消化不良[12]。后两类患者虽然有Hp 感染,但根除后症状无改善或仅有短时间改善(后者不排除根除方案中PPI 的作用),因此仍可视为功能性消化不良(图1)。所以,Hp 相关消化不良是一种独特的疾病实体,即与根除Hp 后症状无改善或仅短时间改善的患者不同,应归于器质性消化不良范畴,这一归类方法不同于传统归类方法,显得更为科学、客观。
3. 根除Hp 应作为消化不良处理的一线治疗【陈述9】【陈述10】【陈述11】
早在2005 年,美国胃肠病学会关于消化不良处理方案的全面评估报告中就指出:总体而言,在功能性消化不良治疗中已确立疗效(与安慰剂治疗相比)的方案仅仅是根除Hp 和PPI 治疗;对于Hp 阳性患者,根除治疗是最经济有效的方法,因为一次治疗可获得长期效果[13]。“ 京都全球共识”仅仅是重申了根除Hp 对消化不良症状的疗效高于安慰剂这一事实和推荐其作为一线治疗的观点。事实上,不仅美国,欧洲、亚洲以及一些已制订相关指南的国家均强烈推荐根除Hp 作为消化不良的一线治疗,有高级别证据支持[11]。“ 一线治疗”体现在:①未经调查消化不良(uninvestigated dyspepsia)的处理采用Hp“检测和治疗”策略(test & treat strategy);②因消化不良症状行内镜检查,诊断为慢性胃炎( 即明确为功能性消化不良)者检测Hp,阳性者首先行根除治疗,根除后仍有症状者再采取相应治疗。
根除Hp 作为消化不良处理的一线治疗不仅疗效相对较高,而且可以预防消化性溃疡和胃癌,减少传染源。我国“ Hp 感染处理共识”(2007、2012年)[14]和“慢性胃炎共识意见”(2006、2012 年)[15]中均推荐对Hp 阳性慢性胃炎伴消化不良( 相当于Hp 阳性的功能性消化不良)者行根除治疗。鉴于我国内镜检查普及率高、检查费用低且上消化道肿瘤发病率高,未推荐“ 检测和治疗”策略。我国“ 消化不良诊治指南”(2007 年)处理流程图中未提及Hp[16],显然不妥。我国学者撰文“ 重视根除Hp 处理在消化不良处理中的应用”[17],详细阐述了根除Hp 应作为消化不良处理的一线治疗的观点,惜未引起国内学者重视( 极少被引用;不少消化科医师在消化不良患者的处理中不检测Hp)。
综上所述,推荐根除Hp 作为消化不良处理一线治疗的理由充分,而且显而易见:疗效确实(安慰剂对照研究证实),一次治疗可获得长期效果。当然实施这一策略时也需要注意个体化,在高龄、伴存严重疾病等患者中,根除Hp 不适合作为一线治疗。
三、胃炎的诊断评估
Hp 胃炎的发展与胃炎、萎缩和肠化生分布部位及其严重程度密切相关。胃体为主的萎缩性胃炎,尤其是程度严重时,胃癌发生风险显著增加;而胃窦为主的胃炎患者中十二指肠溃疡的风险增加。ICD 中的胃炎分类仅是粗略分类,需要细化。
1、基于悉尼分类评估【陈述3】【陈述4】【陈述5】
胃炎分类的悉尼系统( Sydney System)(1991年)[18]将慢性胃炎分为全胃炎、胃窦炎和胃体炎。事实上,多数胃炎并不仅局限于胃窦或胃体,因此,此后全胃炎衍生出胃窦为主胃炎( antrum-predominantgastritis)和胃体为主胃炎( corpus-predominantgastritis)。胃炎分类的新悉尼系统( Updated SydneySystem)(1994 年)[19]强调了胃黏膜活检部位和活检块数(胃窦大、小弯各1 块,胃角1 块,胃体大、小弯各1 块),对炎症、活动性、萎缩、化生和Hp 感染的严重程度分级(0、1、2、3)提出了直观模拟评分(visual analogue scales),便于评估,减少了观察者之间的评分差异。我国“ 慢性胃炎共识意见”(2006、2012 年)[15]采纳了这些国际分类精要。
慢性胃炎分类中,国内慢性胃炎共识意见将糜烂与胃炎分开描述[15],糜烂在Hp 胃炎中的意义尚不明确。
2、胃黏膜萎缩程度和范围评估【陈述12】【陈述13】
胃黏膜萎缩分为单纯性萎缩和化生性萎缩,即肠化生也属于萎缩[19]。
(1)内镜观察:常规内镜下观察无法准确诊断胃黏膜萎缩和化生[15],必须进行组织活检,并依据悉尼分类标准对胃黏膜行组织形态学评估。然而,影像增强内镜检查(image-enhanced endoscopy)在诊断胃黏膜萎缩/ 肠化生方面具有较高的准确性和可重复性[20-22]。影像增强内镜包括色素内镜、高分辨率放大内镜和结合放大技术的影像增强内镜。如用影像增强内镜检查指导黏膜活检,可进一步提高萎缩黏膜和肠化生检查的准确率。但目前除日本外,尚未普遍开展这类检查。
(2)OLGA 和OLGIM 胃癌风险分期方法【陈述14A】【陈述14B】:OLGA( operative link for gastritisassessment,意译为“可操作的与胃癌风险联系的胃炎评估”)和OLGIM( operative link for gastric intestinalmetaplasia assessment,意译为“ 可操作的与胃癌风险联系的肠化生评估”)是由慢性胃炎分类新悉尼系统发展而来的胃癌风险分期方法[23-24]。按照慢性胃炎新悉尼系统要求活检,每块活检标本观察10 个腺体,根据观察腺体中的萎缩( OLGA)或肠化生(OLGIM)腺体个数,计算萎缩(包括肠化生)或肠化生区域( 仅肠化生)。OLGA 或OLGIM 分期Ⅲ或Ⅳ者,属于胃癌高风险患者[4]。OLGIM 评估的重复性和与胃癌发生风险的关联性优于OLGA( 萎缩判定有主观性,肠化生易于识别)[25]。这是目前评估胃黏膜萎缩/ 肠化生准确性相对较高的方法。OLGA 分期见图2。
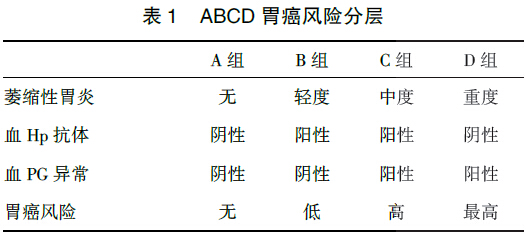
(3)非侵入性ABC 法【陈述15】:这是一种非侵入性筛查方法,通过测定血Hp 抗体和血胃蛋白酶原(PG)Ⅰ、PGⅡ水平将受检者分成A、B、C、D 四组。血PG Ⅰ和PG Ⅰ/Ⅱ水平降低的异常改变提示存在胃黏膜萎缩。分组方法和各组胃癌发生风险见表1。如果能以经过当地验证的临界值( cut-offvalue)作为标准,可以发现胃癌发生风险增加的个体,主要用于筛查[26]。
四、Hp 胃炎的处理
1、 Hp 感染者应给予根除治疗,除非有抗衡方面考虑【陈述17】
上文已述,Hp 感染几乎均会发生慢性活动性胃炎,即Hp 胃炎;Hp 胃炎是一种感染性疾病,更确切地说是一种传染病。虽然多数Hp 胃炎患者既无消化不良症状,最终也不发生消化性溃疡、胃癌、胃MALT 淋巴瘤等严重疾病,但究竟谁最终会在Hp 胃炎的基础上发生严重疾病难以预测,这种情况类似于无症状的结核或梅毒感染。而且早期胃癌症状隐匿,发现时多已属中、晚期,预后不良。根除Hp可有效预防和治疗Hp 相关消化不良、消化性溃疡,在较大程度上预防胃癌发生。此外,Hp 感染始终具有传染性,根除Hp 可减少传染源。30 余年来全球范围内大量患者的根除治疗结果证明,根除Hp 后的负面影响(可能会增加胃食管反流病、肥胖、哮喘等疾病发病率以及造成人体菌群紊乱等,但这些尚有争议)远远低于上述正面作用[4]。为此,Hp 感染者应给予根除治疗,除非有抗衡方面考虑。抗衡因素包括患者伴存疾病、社区中高再感染率、卫生资源优先度安排等。
2、根除Hp 可降低胃癌发生风险【陈述18】【陈述20】【陈述22】
根除Hp 预防胃癌的对照研究和meta 分析结果显示,根除Hp 可降低胃癌发生风险,风险降低程度取决于根除治疗时的胃黏膜萎缩严重程度和范围[27-28]。根除治疗时未发生胃黏膜萎缩者,根除 Hp 后几乎可以完全预防肠型胃癌的发生;对已有胃黏膜萎缩者则预防效果降低或显著降低。无症状个体在胃黏膜仍处于非萎缩阶段时根除Hp 获益最大,因为此阶段根除治疗可有效预防Hp 相关消化不良、消化性溃疡和胃癌。随访研究显示,根除Hp后胃黏膜炎症消退,萎缩/ 肠化生发展可以停止或减缓;部分萎缩可以逆转,但肠化生不能逆转[29]。也就是说,根除Hp 作为降低胃癌发生风险的一级预防措施并不能消除已有胃黏膜萎缩/ 肠化生者的胃癌发生风险,这些患者需要进行二级预防,即随访和处理[26]。
3、根除Hp 方案应根据各地不同情况选择【陈述19】
随着Hp 耐药率的上升,标准三联疗法的根除率已显著下降。不同国家或地区的Hp 耐药率、药物可获得性、经济条件等存在差异,因此根除方案的选择应根据各地不同情况,基于药敏试验结果治疗和经验治疗是抗感染治疗的两种基本策略。定期监测人群抗菌药物耐药率,可为经验治疗抗菌药物的选择提供依据;是否实施基于药敏试验结果的个体化治疗,很大程度上取决于经验治疗的成功率。目前推荐的经验性铋剂四联方案[14]和在无铋剂条件下推荐的非铋剂四联方案( 尤其是伴同疗法)仍可在很大程度上克服克拉霉素、甲硝唑和左氧氟沙星耐药;而阿莫西林、四环素、呋喃唑酮耐药率仍极低,应用前不需要行药敏试验。Maastricht Ⅳ共识[5]和我国最新共识[14]均推荐在二次治疗失败后进行药敏试验,但实际作用可能有限。
4、Hp 是否根除成功需要评估【陈述21】鉴于Hp 根除率在下降中且未根除者仍存在严重疾病发生风险,推荐所有患者均应在根除治疗后进行复查。复查最好采用非侵入方法,包括尿素呼气试验和粪便Hp 抗原试验,常用前者。Hp 根除治疗后复查收集的资料也可用于根除方案疗效评估。
5、 胃癌高风险患者根除Hp 后仍需随访
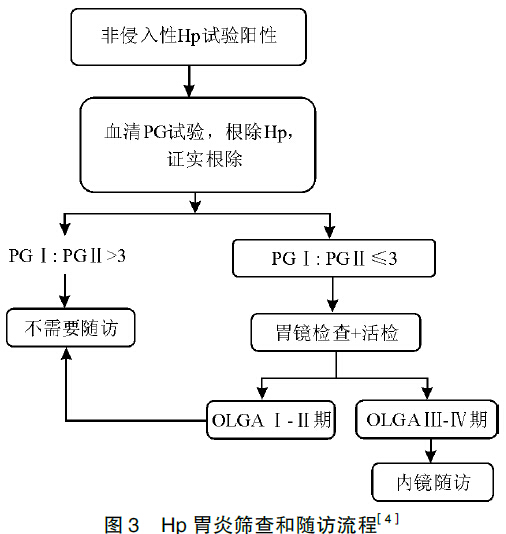
根除Hp 时已有胃黏膜萎缩/ 肠化生,尤其是程度较重、范围较广的患者,根除Hp 后仍属胃癌高风险患者,需要定期内镜检查随访。这些患者包括胃癌风险评估指标OLGA Ⅲ或Ⅳ期,或PG≤70 ng/ mL和PGⅠ: PGⅡ ≤3[4](参见上文“胃黏膜萎缩程度和范围评估”)。此外,早期胃癌内镜下切除术后或有异型增生( 上皮内瘤变)者亦需密切随访。ABC法与OLGA 法结合筛查和随访的相关流程见图3。
6、搜寻( search)和筛查( screen)Hp 胃炎何时合适?【陈述16】
搜寻可能仅指发现Hp 胃炎患者,筛查包含了发现胃癌高风险患者。搜寻和筛查Hp 胃炎的合适时间为萎缩和肠化生发生前,人群中Hp 胃炎患者发生胃黏膜萎缩/ 肠化生的年龄需要通过流行病学调查确定。Hp 感染多数发生在儿童时期,12 岁以后较少发生感染,多数感染通过家庭内传播。日本是世界上胃癌发病率最高的国家,流行病学调查显示,Hp 感染者20 岁以后就有部分患者发生萎缩/ 肠化生[30]。因此他们提出,出于预防胃癌目的,合适的搜寻Hp 胃炎年龄为12 ~ 20 岁。我国胃癌发病率存在显著的地区差异,Hp 感染率总体上仍很高,感染后发生胃黏膜萎缩/ 肠化生的年龄尚不清楚,根除后再感染率也可能较高,因此合适的搜寻和筛查Hp 胃炎年龄有待确定。
展开部分内容仅可在
临床指南app 查看下载
收藏
分享


















